前列腺癌是全球男性发病率第二、致死率第五的恶性肿瘤,其进展通常由雄激素驱动,临床惯用雄激素剥夺疗法(ADT)以阻断雄激素作用,但部分患者仍会持续进展并出现远处转移。数据显示,约10%–20%的前列腺癌患者会在5年内发展为去势抵抗性前列腺癌(CRPC),其中84%的患者确诊时已转移,即便是无转移患者,也有约33%可能在2年内出现骨转移1。
对于转移性CRPC,NCCN指南推荐的一线方案为新型激素(内分泌)治疗与化疗。然而在新型激素和化疗治疗失败后,后续可选方案虽包含PARP抑制剂、免疫治疗及放射性药物,但疗效普遍有限,临床上仍缺乏广泛适用且效果明确的后线治疗手段2,3。

TROP2 ADC探路mCRPC,sac-TMT+K药显积极信号
ADC药物凭借“精准递送+强效杀伤”的双重机制,已成为实体瘤治疗绕不开的探索方向。而TROP2靶点因在前列腺肿瘤细胞中表达率高达71%,被视为重要的潜在靶点。
根据ESMO官网的披露信息,科伦博泰与默沙东合作开展的2期研究(SKB264-II-06/MK-2870-002)——TROP2ADC芦康沙妥珠单抗(sac-TMT)联合帕博利珠单抗(pembro)治疗mCRPC公布了研究摘要,引起了行业关注。
该研究队列D共纳入46例经1或2种新型内分泌治疗及≤1种化疗治疗的患者,其中10例接受sac-TMT 4mg/kg + pembro治疗,中位随访时间为10.8个月;36例接受sac-TMT 5mg/kg + pembro治疗,中位随访时间为12.9个月。
安全性方面,两个剂量组均未发生剂量限制毒性(DLT),4 mg/kg组未发生治疗相关死亡,5 mg/kg组出现1例治疗相关死亡。疗效数据如下表(数据截至2024年11月18日):
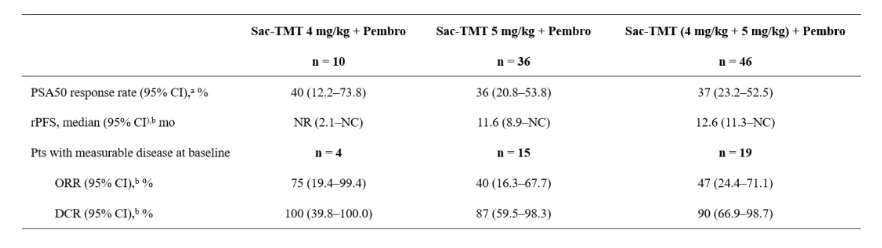
数据表明,sac-TMT联合pembro在mCRPC人群中具有良好的抗肿瘤活性与可管理的安全性。
值得一提的是,其他mCRPC二线推荐疗法,如Pluvicto、多西他赛、卡巴他赛、奥拉帕利、镭-223、恩扎卢胺/阿比特龙,rPFS总体在5.6-9.3个月4。对比来看,sac-TMT联合疗法rPFS在11.6-12.6个月,DCR达87%-100%,在二线及以上治疗场景中优势明显。
ADC竞逐mCRPC,联合疗法优势突出
同为TROP2 ADC药物的戈沙妥珠单抗(SG),目前也针对mCRPC开展了临床研究。其用于经ARIS治疗mCRPC(22%接受过多西他赛化疗)的2期研究数据显示:总人群rPFS为6.1个月,6个月rPFS率为52%;在未经化疗的亚组中,rPFS为8.3个月,6个月rPFS率为68%。此外,SG单药治疗组未观察到PSA50应答,而3例接受SG +ARSI治疗的患者中有2例出现PSA50应答5。
除了TROP2靶点,PSMA、B7H3等靶点的ADC药物也是mCRPC后线治疗的重要探索方向。
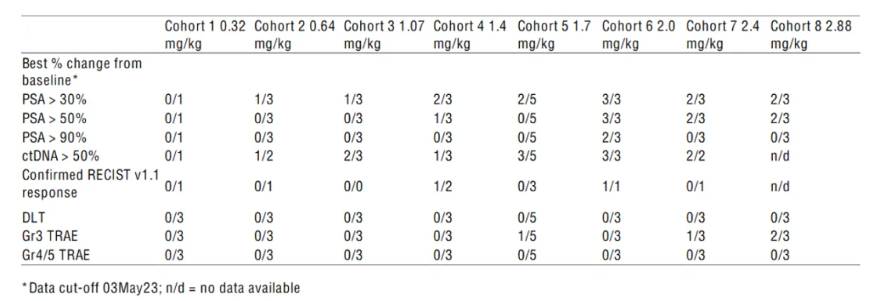
由Ambrx(后被强生收购)开发的PSMA ADC药物ARX517,其治疗mCRPC患者1/2期研究结果曾于2023 ESMO大会上公布。入组患者100%接受过≥1种激素治疗,50%接受过紫杉烷类药物,12.5%接受过PSMA靶向放射性核素治疗,在较高剂量组(1.4mg/kg-2.88mg/kg)中,可观察到>50%的PSA和ctDNA下降;2例患者(2/7)达到经RECIST v1.1标准确认的客观缓解6。
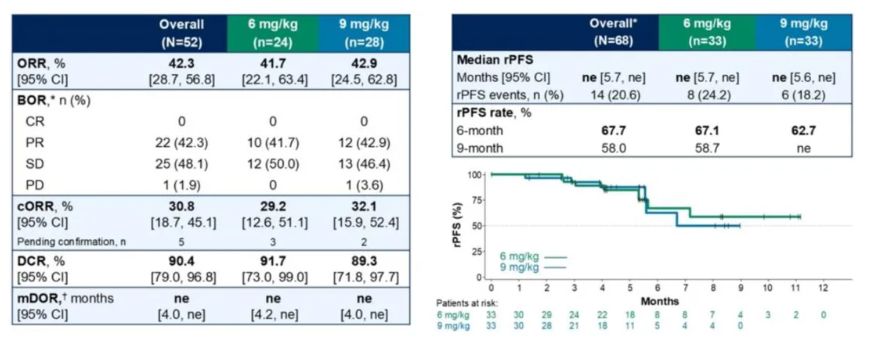
映恩生物则在今年ASCO会议上汇报了B7H3 ADC药物DB-1311治疗mCRPC的1/2期临床数据。大多数患者接受过多西他赛(93.2%)及激素治疗(95.9%),其他治疗包括PARP抑制剂(13.7%)、Lutetium-177(21.9%)及免疫治疗(16.4%)。在可评估疗效的患者中,cORR为30.8%,DCR为90.4%,6个月rPFS为67.7%。
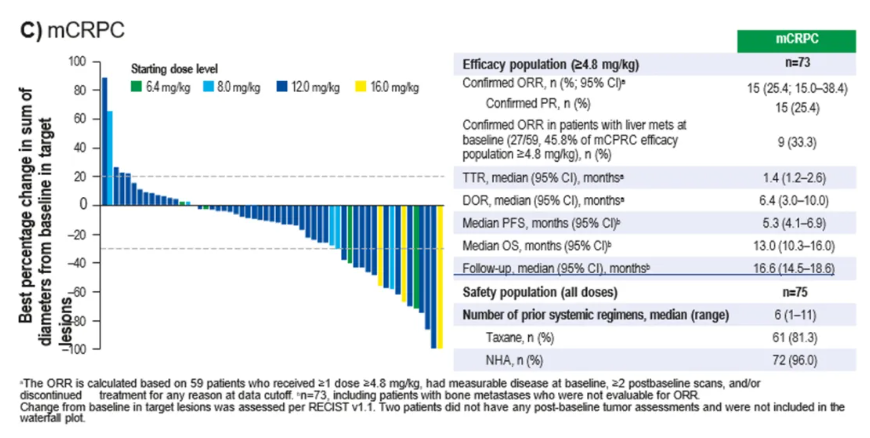
而第一三共与默沙东联合开发的另一款B7H3 ADC药物DS-7300,其1/2期数据显示,mCRPC后线患者的ORR为25%,mPFS为5.3个月,mOS为13.0个月,DOR为6.4个月7。
从同靶点ADC药物的数据来看,TROP2 ADC联合疗法(无论是与免疫疗法联用还是与ARSI联用),相比单药治疗能有更高的PSA应答率,也更有可能改善患者的生存获益;而进一步扩展至不同靶点,sac-TMT联合疗法始终在ORR、rPFS的关键指标上保持领先,体现出更强的抗肿瘤效果与疾病控制能力,这将为改善患者生存质量带来切实意义。
打破免疫治疗困局,“ADC +IO”成突破口
前列腺癌因肿瘤突变负荷低、免疫浸润不足,使其对免疫治疗单药反应有限,被称为“冷肿瘤”。
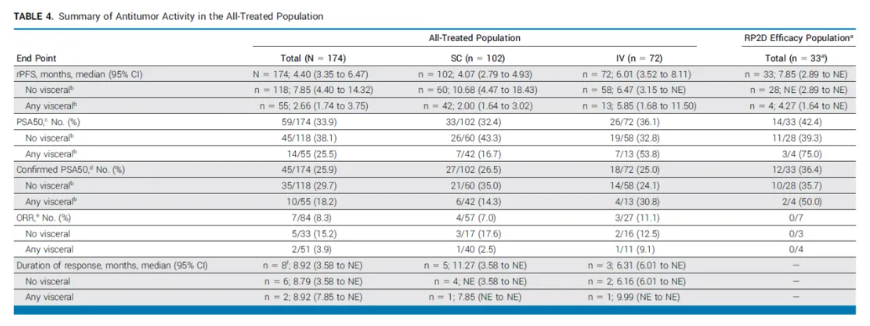
今年ASCO会议上,强生公布了KLK2/CD3双抗Pasritamig治疗mCRPC的1期临床数据,在推荐剂量(RP2D)下,33例患者的rPFS为7.85个月,PSA50响应比例为42.4%,而在84例可评估患者中,ORR仅8.3%。目前,强生已启动Pasritamig + PSMA ADC的1b期临床研究,从侧面印证了联合疗法对强化前列腺癌免疫治疗的必要性。
而身为“PD-1之王”的pembro,也早早在mCRPC中开启了一系列探索,但结果并不理想——其单药治疗在PD-L1阳性患者中的ORR为5%,在PD-L1阴性患者中的ORR仅为3.5%,对应的mOS为9.5个月和7.9个月;此外,其联合化疗治疗mCRPC的3期研究(KEYNOTE-921)未能达到主要终点,与PARP抑制剂、紫杉类化疗、雄激素剥夺疗法等其他方案的联合治疗,也未显示出显著疗效8。
在此背景下,“ADC+IO”的联合策略被视为新的突破口。这次ESMO公布的sac-TMT联合pembro的临床数据,正是两者机制协同产生的积极成果——尽管pembro单药在mCRPC中的疗效有限,但在联合sac-TMT后,关键疗效指标有了明显提升,这为pembro在久攻不下的适应症中开辟了新的治疗可能。
结语
作为国产TROP2 ADC的代表,芦康沙妥珠单抗已在乳腺癌、肺癌等领域成功突围,并持续向更前线、更广泛的适应症拓展。
基于对科伦博泰临床研究能力及产品应用潜力的认可,默沙东通过license-in获得了芦康沙妥珠单抗的海外权益,并为其布局了14项全球3期临床。这次联合治疗研究,是科伦博泰与默沙东共同开展的多项全球2期篮子研究之一,除mCRPC之外,这些篮子试验还将支持芦康沙妥珠单抗开展覆盖多种实体瘤的关键性研究。
期待“芦康沙妥珠单抗+K药”这一双王组合,能在更大样本与更高证据级别的研究中得以验证,在为前列腺癌患者提升生存质量的同时,也为更多癌种治疗提供可复制的“ADC+IO”方案,真正地实现“以中国创新,定义全球标准”。
参考材料:
[1] Kirby M, Hirst C, Crawford ED. Characterising the castration-resistant prostate cancer population: a systematic review. Int J Clin Pract. 2011 Nov;65(11):1180-92. doi: 10.1111/j.1742-1241.2011.02799.x. PMID: 21995694.
[2] Vir Biotechnology Q2:24 Investor Conference Call
[3] Cimadamore A, Boixareu C, Sharp A, et al. Novel Therapeutic Strategies for Metastatic Prostate Cancer Care[J]. European Urology, 2025.
[4] 太平洋证券:聚焦肿瘤和代谢领域的创新先锋
[5] https://www.askgileadmedical.com/docs/trodelvy/trodelvy-use-in-metastatic-castration-resistant-prostate-cancer-progressing-on-androgen-receptor-signaling-inhibitors/pdf
[6] https://www.annalsofoncology.org/article/S0923-7534(23)03589-5/fulltext
[7] https://www.daiichisankyo.com/files/investors/library/materials/2023/ESMO%202023%20Highlight%20IR%20conference%20call_Final%20Oct%2024.pdf
[8] Cimadamore A, Boixareu C, Sharp A, et al. Novel Therapeutic Strategies for Metastatic Prostate Cancer Care[J]. European Urology, 2025.

